圣彼得堡国立大学医学团队研发小鼠模型,助力开发治疗人类失明新方法
圣彼得堡大学的科学家们利用先进的“分子剪刀”技术,精确地模拟了人类色素性视网膜炎在小鼠身上的表现。色素性视网膜炎是一种严重的眼部疾病,如果不及时治疗,可能导致患者逐渐失去视力,最终发展为不可逆的失明。这些小鼠模型的创建,将为临床前药物试验提供重要支持。
视网膜变性病是一类慢性进展性疾病,随时间推移会导致视力显著下降。其严重之处在于,有时由于光感受器的丧失或功能障碍,视力损伤可能达到不可逆的程度。在这一疾病谱系中,泛发性视网膜损伤尤为严重,其中色素性视网膜炎便是其典型代表之一。
目前已知,人类色素性视网膜炎与70多个不同基因中的数千个突变有关。其中,pde6b基因的突变会导致一种遗传性视网膜萎缩,可能引发不可逆的失明和劳动年龄时的残疾。为应对这一问题,俄罗斯谢秋诺夫科学院进化生理学和生物化学研究所的科学家们正积极研发光遗传学视网膜植入药物。为此,他们向圣彼得堡大学的研究人员提出合作请求,希望为深入研究色素性视网膜炎创建一系列模型小鼠。
研究结果发布在 International Journal of Molecular Sciences
基因传导与基因编辑技术中心主任叶莲娜·列奥诺娃表示:“我们运用CRISPR/CAS9基因编辑技术成功在小鼠中构建了该疾病的模型。这一技术精准地利用CAS蛋白与特定RNA分子的结合,对基因组进行精确修改。在圣彼得堡大学的转基因与基因编辑中心,我们完成了整个CRISPR/CAS技术流程,即从获取和纯化重组CAS核酸酶,到最终获得基因编辑后的小鼠。”
当前,针对这一疾病群体的特异性有效治疗手段在广泛的临床实践中仍显不足。为了填补这一空白,科学家们致力于开发特殊的模型小鼠,以模拟疾病在人类眼中的临床表现,进而为未来的治疗策略探索提供有力支持。选择小鼠作为研究模型的原因在于,其眼睛结构与人类高度相似,同样容易受到各种病理影响。
哺乳动物的视网膜由三层结构组成,涵盖了多种类型的细胞。光线依次穿过角膜、瞳孔、晶状体和玻璃体,最终抵达视网膜的光感受器层。这些光感受器细胞负责将光能转化为电信号。随后,其他类型的视网膜细胞对这些信号进行加工处理,并通过视神经传递到大脑进行最终的图像解析。
这个过程对于鼠类和人类来说是一样的。在视网膜变性疾病中,光感受器细胞的死亡是导致失明的关键因素,而其他视网膜层则往往保持相对完整。
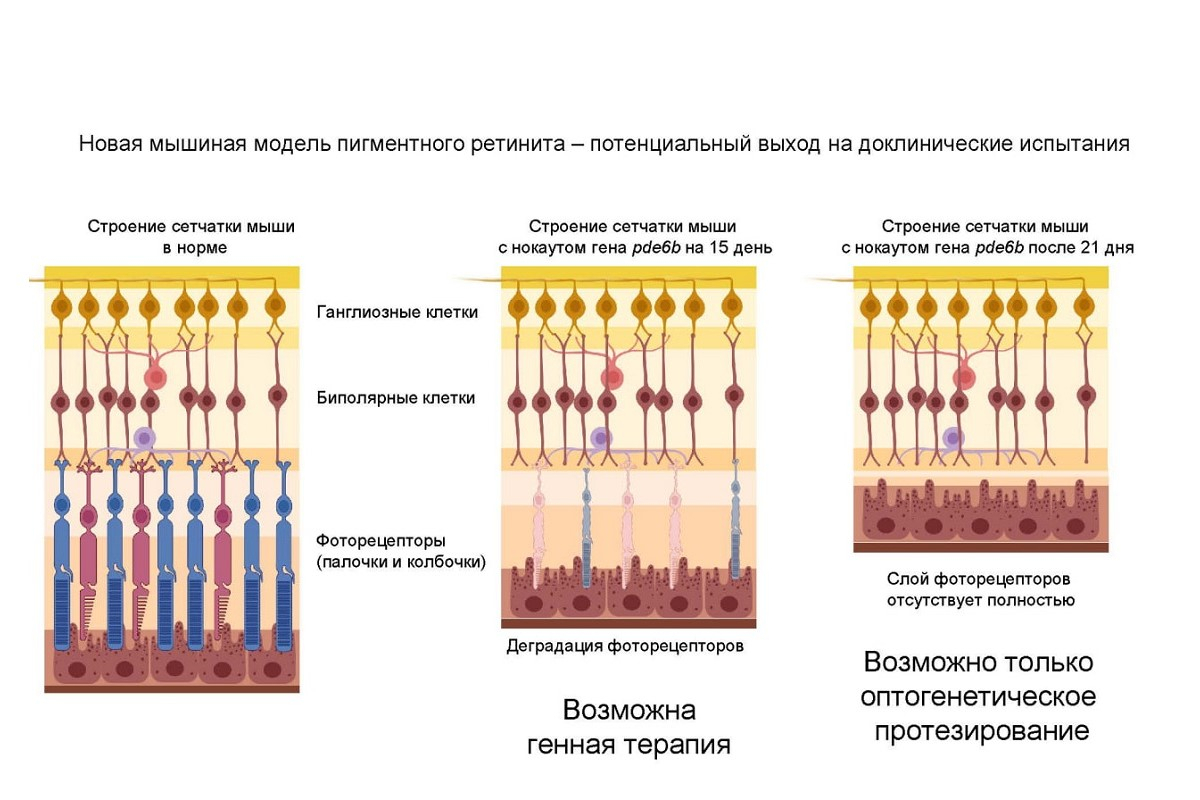
研究人员在本校成功创建了小鼠模型,以深入研究特定疾病对视网膜细胞的影响。据观察,模型小鼠在出生后的第15天开始出现视网膜细胞死亡,至第21天时,视网膜中的光感受器层已完全消失。本校科学家们认为,对这一小鼠模型的研究将为基因替代疗法和光遗传学视网膜植入的临床前研究提供重要支持。
基因替代疗法药物中包含健康的基因副本,该基因副本能够在存活的光感受器细胞中生成功能性Pde6b蛋白,从而避免疾病的影响。而光遗传学视网膜植入技术则通过在双极细胞中生成光敏蛋白,作为将视觉信息传递给大脑的替代途径。

