圣彼得堡国立大学的科学家明确了辐射破坏肠道上皮屏障的机制
圣彼得堡国立大学的生物学家发现,电离辐射会损害肠道上皮屏障特性的主要调节剂claudin-2,并已确定防止该种损害的有前景性的办法。
核电厂事故及长期太空飞行期间的电离辐射会对身体造成严重后果。然而,恰恰是此类辐射暴露在肿瘤疾病的治疗中起着重要作用。在治疗过程中,辐射通常会扩散到肿瘤区域之外,从而导致临近器官受到影响。
研究成果发表于 International Journal of Molecular Sciences.
电离辐射对健康器官的影响之一是肠道区急性放射病。为了研究肠道各部分对辐射的反应,科学家首先对模型动物进行了实验,以便查明常见的及特定的功能障碍分子机制——先是在动物中,今后在人类中。
在对大鼠的实验中,圣彼得堡国立大学的科学家们专注于研究关键蛋白质,这些蛋白质保障了肠上皮细胞的机械连接,并能调节其中的细胞间运输。肠上皮作为细胞的集合,创造了一个屏障,保护肠道免受有害物质和病原体的影响。
圣彼得堡国立大学的生物学家研究了claudine蛋白,其组合形式及水平变化会导致上皮屏障特性发生改变。据研究人员介绍,某些claudins水平的增加表明肠道屏障通透性的提升,而另外一些claudins的存在则预示着细胞的适应性反应。了解这些依赖关系可帮助科学家确定电离辐射对肠道功能障碍的影响机制,这在未来可能成为选择治疗方案的最重要因素。
“我们获得了关于这些蛋白质在肠道各段变化性质的优先数据,并揭示了其对辐射的反应。最重要的成果是确定了辐射对肠上皮屏障特性的主要调节剂,即所谓的claudin-2的破坏作用。”
圣彼得堡国立大学(普通生理学系)教授亚历山大·马尔科夫和伊戈尔·克里沃伊
该研究是圣彼得堡国立大学科学家前期项目——“Na,K-Atp酶和claudines的分子多样性及功能相互作用”——的延续,后者荣获圣彼得堡国立大学“重大科研成果奖”。
Na,K-Atp酶是一切动物细胞质膜的转运蛋白,对其功能至关重要。除了Na离子易位的传统功能之外,K-Atp酶在与植物来源物质ouabain分子相互作用时,可触发神经元、肌肉和上皮细胞中的许多信号通路。
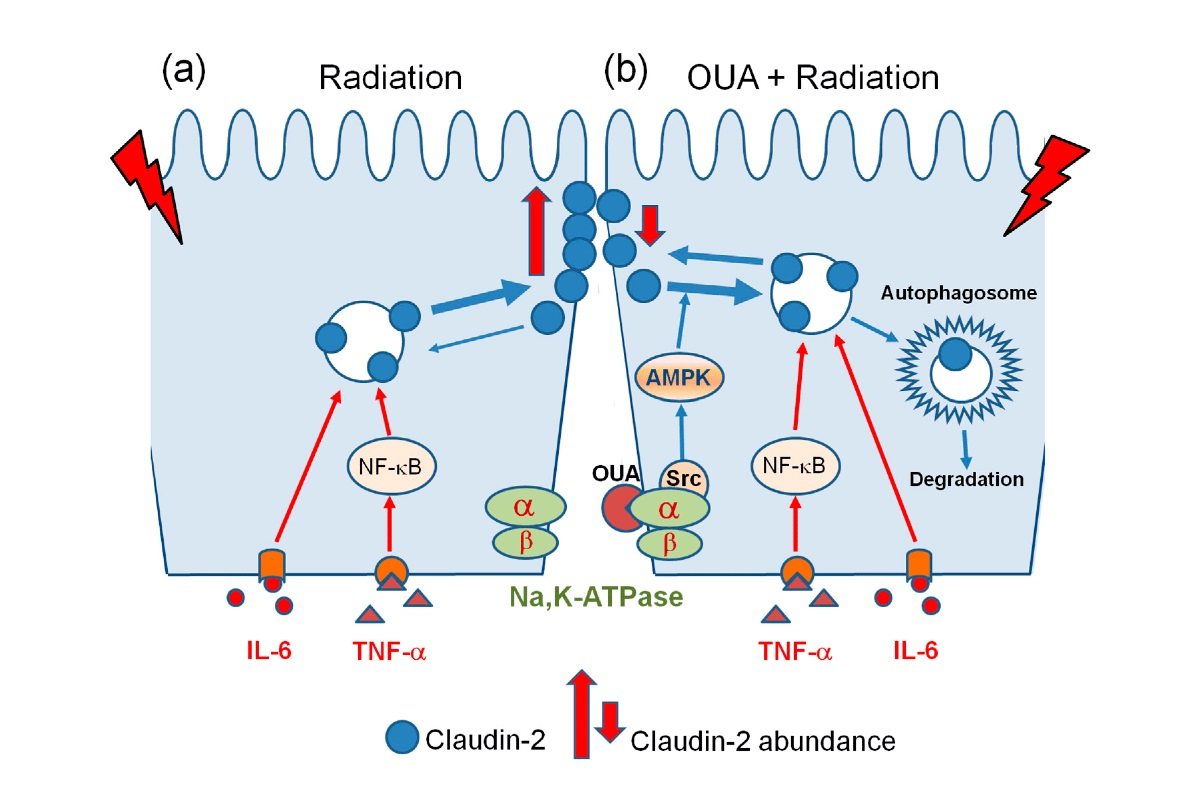
“Ouabain水平的变化和启动的信号反应在各种生理和病理生理学条件下对表皮组织及整个身体具有重要的适应性意义,并表现为神经保护、抗癌和抗病毒等作用。我们的研究首次在大鼠辐射损伤的条件下,通过注射ouabain来提高其在血液中的水平,并揭示了这种作用对claudine-2和肠上皮屏障特性的保护效果。”研究者介绍道。
在这项工作中,圣彼得堡国立大学的科学家们开发了一种ouabain保护作用的分子机制方案。研究成果未来可用于研发防治炎症性疾病及其他肠道疾病的新方法,包括临床实践以及长期太空飞行期间辐射增加的问题。

